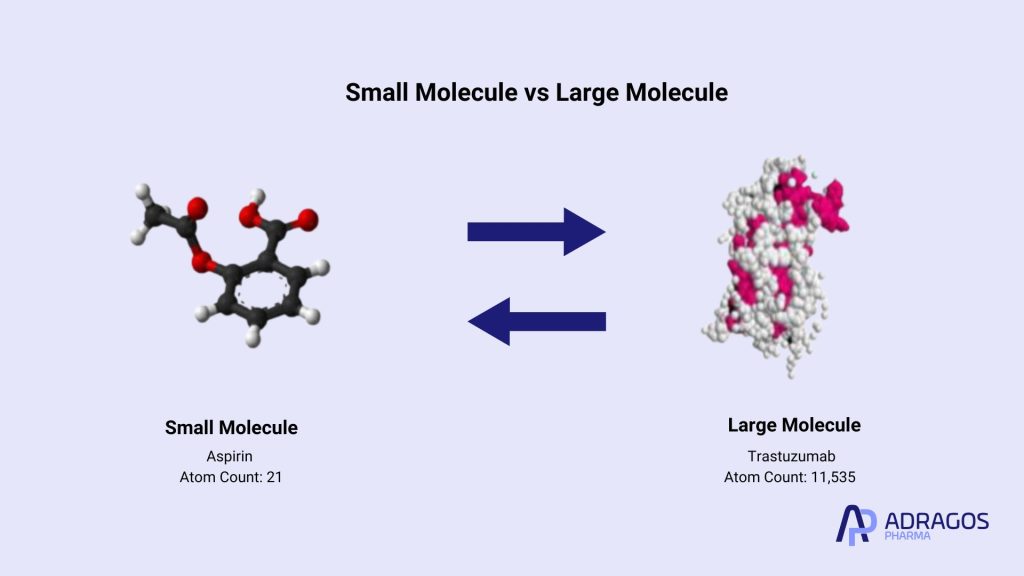
L’industrie pharmaceutique repose sur deux types principaux de médicaments : les molécules de petite taille et les molécules de grande taille. Les deux jouent des rôles essentiels dans la médecine moderne, mais diffèrent considérablement en termes de structure, de fonction et de méthodes de production. La compréhension de ces différences entre les molécules de petite et de grande taille est cruciale pour les professionnels impliqués dans le développement de médicaments et les processus de fabrication.
Cet article explore les caractéristiques des molécules de grande taille, leur comparaison avec les molécules de petite taille, et leur impact sur le développement de médicaments pharmaceutiques.
Définir les molécules de grande taille : caractéristiques et importance
Que sont les molécules de grande taille ?
Les molécules de grande taille, ou produits biologiques, ont un poids moléculaire élevé et sont fabriquées ou extraites d’organismes vivants. Elles sont composées de protéines à structure complexe et beaucoup moins stables que les médicaments à petites molécules. Contrairement aux médicaments à petites molécules, qui sont principalement synthétisés chimiquement, les molécules de grande taille sont dérivées de cellules vivantes. Leur complexité leur permet de cibler des processus biologiques spécifiques avec une grande précision, les rendant très efficaces dans le traitement de diverses maladies, notamment le cancer et les troubles auto-immuns. La caractérisation efficace des produits biologiques repose fortement sur un développement de processus robuste pour garantir des résultats fructueux de manière appropriée à chaque phase.
Caractéristiques clés des molécules de grande taille
- Poids moléculaire élevé : Généralement plus grandes que les médicaments à petites molécules, nécessitant des techniques analytiques spécialisées telles que la spectrométrie de masse (LC-MS) et la chromatographie d’exclusion stérique.
- Origine biologique : Produites à l’aide d’organismes vivants, nécessitant souvent le développement de lignées cellulaires et des processus en amont/aval.
- Structures complexes : Impliquent des liaisons chimiques complexes et des modifications post-traductionnelles qui affectent la fonction et la stabilité.
- Mode d’action spécifique : Souvent conçues pour interagir avec des cibles cellulaires particulières, comme les anticorps monoclonaux qui se lient aux antigènes.
- Biodisponibilité orale limitée : En raison de leur taille et de leur instabilité dans le système digestif, la plupart des médicaments à grandes molécules sont administrés par injection ou perfusion intraveineuse.
Molécules de petite taille : une comparaison
Que sont les molécules de petite taille ?
Les molécules de petite taille sont des composés de faible poids moléculaire qui peuvent être synthétisés par chimie organique. Elles constituent la base de nombreux médicaments pharmaceutiques traditionnels, y compris les antibiotiques, les analgésiques et les médicaments cardiovasculaires.
En quoi les molécules de petite taille diffèrent-elles des molécules de grande taille ?
Taille et poids moléculaire : Les molécules de petite taille ont généralement un faible poids moléculaire, leur permettant de diffuser facilement à travers les membranes cellulaires.
Synthèse chimique : Contrairement aux molécules de grande taille, qui nécessitent des cellules vivantes pour leur production, les molécules de petite taille sont généralement créées par des processus de synthèse de médicaments bien établis.
Administration du médicament : De nombreux médicaments à petites molécules peuvent être pris par voie orale, tandis que les molécules de grande taille nécessitent des systèmes d’administration de médicaments spécialisés.
Considérations réglementaires : Les molécules de petite taille ont généralement des voies d’approbation FDA plus simples par rapport aux molécules de grande taille, qui subissent des tests approfondis pour l’immunogénicité, les tests de liaison, et les phases d’essais cliniques.
Bien que les médicaments à petites molécules restent largement utilisés, les molécules de grande taille sont devenues de plus en plus importantes en raison de leur capacité à traiter des maladies qui avaient auparavant des options de traitement limitées. Maintenir l’intégrité des molécules de grande taille tout au long du processus analytique est crucial pour garantir des résultats précis et fiables.
Le processus de fabrication des molécules de grande taille
Production par cellules vivantes
Le développement de médicaments à grandes molécules est considérablement plus complexe que la production de médicaments à petites molécules. Étant donné que les molécules de grande taille sont généralement dérivées de cellules vivantes, le processus de fabrication implique plusieurs étapes critiques, notamment :
- Développement de lignées cellulaires : Sélection et optimisation de lignées cellulaires capables de produire la protéine ou l’anticorps monoclonal requis.
- Traitement en amont : Culture des cellules dans des bioréacteurs dans des conditions contrôlées pour maximiser la production de protéines.
- Traitement en aval : Utilisation de techniques telles que la chromatographie d’échange d’ions et la chromatographie en phase inverse pour purifier le médicament à grandes molécules.
- Contrôle qualité : Assurer l’intégrité des données et la cohérence du poids moléculaire, de la structure chimique et de l’activité biologique.
Le développement de médicaments pharmaceutiques à base de molécules de grande taille nécessite un développement de méthodes sophistiqué pour maintenir la stabilité et l’efficacité.
Le rôle des molécules de grande taille dans le développement de médicaments
Anticorps monoclonaux et protéines thérapeutiques
L’une des avancées les plus significatives dans les thérapeutiques à base de molécules de grande taille a été le développement d’anticorps monoclonaux. Ces protéines conçues en laboratoire sont destinées à reconnaître et à se lier à des antigènes spécifiques, les rendant hautement efficaces pour les thérapies ciblées.
Les exemples incluent :
- Herceptin (trastuzumab) : Utilisé pour le traitement du cancer du sein.
- Humira (adalimumab) : Un anticorps monoclonal qui bloque l’inflammation dans les maladies auto-immunes.
Bevacizumab : Utilisé dans la thérapie du cancer pour inhiber la croissance des vaisseaux sanguins dans les tumeurs.
De plus, les protéines thérapeutiques telles que l’insuline et les facteurs de croissance ont transformé le traitement des troubles métaboliques et génétiques.
Thérapie génique et acides nucléiques
Les récentes avancées en information génétique ont conduit au développement de thérapies à base d’acides nucléiques. Ces molécules de grande taille, y compris l’ADN et l’ARN, jouent un rôle crucial dans les stratégies d’exclusion d’exons pour les maladies génétiques et les thérapies à médiation cellulaire.
Avantages et limites des médicaments à petites et grandes molécules
Considérations d’efficacité et de sécurité
Les médicaments à base de petites et de grandes molécules présentent des avantages et des limites uniques qui doivent être soigneusement pris en compte au cours du processus de développement de médicaments.
Les médicaments à petites molécules sont souvent privilégiés pour leur facilité de synthèse, d’optimisation et d’administration. Leur faible poids moléculaire leur permet de diffuser facilement à travers les membranes cellulaires, les rendant efficaces pour traiter une large gamme de maladies. De plus, de nombreux médicaments à petites molécules peuvent être pris par voie orale, ce qui est pratique pour les patients. Cependant, les petites molécules peuvent également avoir des limitations, telles que des effets hors cible, une toxicité et une biodisponibilité limitée.
Les médicaments à grandes molécules, d’autre part, sont connus pour leur capacité à cibler des voies biologiques complexes et à moduler les réponses immunitaires. Ces médicaments, souvent dérivés de cellules vivantes, peuvent être conçus pour interagir avec des récepteurs cellulaires spécifiques, les rendant très efficaces pour traiter des maladies telles que le cancer et les troubles auto-immuns. Cependant, les grandes molécules présentent également des défis, notamment la difficulté de synthèse et d’optimisation, une biodisponibilité limitée et une immunogénicité potentielle. En raison de leur taille et de leur complexité, les médicaments à grandes molécules sont généralement administrés par injection ou perfusion intraveineuse.
Les considérations d’efficacité et de sécurité sont cruciales lors du développement des médicaments à petites et grandes molécules. Cela implique une évaluation minutieuse des avantages et des risques potentiels de chaque médicament, ainsi que de leurs interactions avec d’autres médicaments et systèmes biologiques. En comprenant ces facteurs, les chercheurs et les cliniciens peuvent développer des traitements efficaces et sûrs pour une large gamme de maladies.
En conclusion, le développement de médicaments à petites et grandes molécules nécessite une compréhension approfondie de leurs avantages et limites, ainsi que de leurs interactions potentielles avec les systèmes biologiques. En considérant attentivement ces facteurs, les chercheurs et les cliniciens peuvent développer des traitements efficaces et sûrs pour une large gamme de maladies.
Défis réglementaires et approbation de la FDA
Complexité de l’approbation des grandes molécules
Étant donné que les grandes molécules sont dérivées d’organismes vivants, leur processus d’approbation par la FDA est plus rigoureux que celui des petites molécules.
Les agences réglementaires exigent des données exhaustives sur :
- Les essais de liaison et les essais de liaison aux ligands pour confirmer la spécificité.
- Les modifications post-traductionnelles qui pourraient affecter l’efficacité.
- Les essais cliniques pour évaluer l’administration du médicament, les tests d’immunogénicité et les mécanismes de libération contrôlée.
Les entreprises doivent également assurer la cohérence dans la production de la substance médicamenteuse, car de légères variations dans le processus de fabrication peuvent avoir un impact sur la sécurité et l’efficacité.
L’avenir des médicaments à grandes molécules
Innovations dans l’administration des médicaments
L’un des plus grands défis dans le développement de médicaments à grandes molécules est l’amélioration de l’administration des médicaments. Les chercheurs explorent de nouvelles approches, telles que :
- Les nanoparticules et les protéines de fusion pour une administration ciblée.
- La fabrication continue pour améliorer l’efficacité et l’extensibilité.
- Des voies d’administration alternatives pour aller au-delà des injections et des perfusions.
Élargissement des possibilités de traitement
La recherche continue dans les thérapeutiques à grandes molécules devrait conduire à des traitements révolutionnaires pour les maladies rares, le cancer et les affections neurologiques. L’essor des biosimilaires – des versions très similaires des médicaments à grandes molécules existants – présente également des opportunités pour rendre ces thérapies plus abordables et accessibles.
La distinction entre les petites molécules et les grandes molécules est fondamentale dans le domaine du développement pharmaceutique moderne. Bien que les médicaments à petites molécules demeurent essentiels pour de nombreuses affections, les grandes molécules ont introduit de nouvelles possibilités en matière de produits biologiques, d’anticorps monoclonaux et de médecine génétique.
Malgré les défis liés à la fabrication, aux considérations réglementaires et à l’administration des médicaments, les grandes molécules demeurent une force motrice pour l’avenir de la médecine. Au fur et à mesure que la recherche progresse, ces médicaments continueront de façonner l’industrie, offrant des solutions innovantes pour certaines des maladies les plus complexes.
Questions fréquemment posées (FAQ) concernant les grandes molécules
Quels sont des exemples de grandes molécules ?
Les exemples incluent les anticorps monoclonaux, les protéines thérapeutiques, les acides nucléiques (ADN, ARN) et les enzymes. Ces médicaments sont largement utilisés dans le traitement du cancer, des maladies auto-immunes et des troubles génétiques.
Comment appelle-t-on les très grandes molécules ?
Les molécules extrêmement grandes sont souvent désignées sous le nom de macromolécules ou de structures covalentes géantes, selon leur composition.
Qu’est-ce qui est considéré comme une grande molécule ?
Une grande molécule est tout composé pharmaceutique ayant un poids moléculaire élevé, généralement dérivé de cellules vivantes, et utilisé dans les produits biologiques. Les exemples incluent les anticorps monoclonaux, les acides nucléiques et les protéines thérapeutiques.
Quel est un exemple de médicament à grande molécule ?
Parmi les médicaments à grandes molécules notables figurent Humira (adalimumab) pour les maladies auto-immunes, Herceptin (trastuzumab) pour le cancer du sein, et l’insuline pour le diabète.
